А. Середа, Р. Зайцев.
В этой статье представлен обзор литературы по лечению множественных повреждений связок коленного сустава. Основную часть обзора составляет перевод работы Gregory C. Fanelli и соавторов Management of Complex Knee Ligament Injuries (опубликовано 2010;92:2235-2246. J Bone Joint Surg Am). Мы позволили себе расширить оригинальную работу, дополнив ее классификацией, несколькими новыми иллюстрациями, более подробным описанием хирургических методик, терминологическими определениями, данными по анатомии и некоторыми другими моментами.
Введение
Понятие множественного (сочетанного) повреждения связок коленного сустава очевидно подразумевает травму нескольких связок. Часто такое повреждение связок возникает в результате вывиха, подвывиха или переломовывиха в коленном суставе, однако эти понятия не являются полностью синонимичными. Прежде всего о множественном повреждении связок говорят тогда, когда мы имеем дело с клинической нестабильностью, а вывих или переломовывих – более «экстренный» ортопедический диагноз. Тем не менее, вывих или переломовывих невозможен без множественного повреждения связок. Если же говорить о вывихе в контексте повреждения связок коленного сустава, то для описания используются термины «вывих голени» и «вывих в коленном суставе». Стоит отметить, что с анатомической точки зрения к вывихам в коленном суставе относятся и вывихи надколенника, но с клинической точки зрения вывихи и нестабильность надколенника следует отнести к отдельной нозологической форме. Поэтому, если в литературе используется термин вывих в коленном суставе, то в в подавляющем большинстве имеются в виду повреждения крестообразных, коллатеральных связок, заднемедиального и заднелатерального углов, а не повреждения связок надколенника.
Многообразие вывихов в коленном суставе определяется характером смещения голени по отношении к бедру, которое чаще всего направлено кпереди (40%) и происходит по типу переразгибания. При этом в 20-50% случаев происходит спонтанное вправление. При таком типе вывиха возможно повреждение подколенной артерии, которая попадает в удавку hiatus tendineus (adductorius) или арки m. soleus.
Задние вывихи (33%) как правило высокоэнергетические. Происходят при ударе спереди по верхней части голени при согнутой ноге в коленном суставе. Иногда при этом повреждается и разгибательный механизм голени, может возникнуть разрыв подколенной артерии.
Медиальные вывихи возникают в 4% случаев, а ротационные обычно носят заднелатеральный характер и также встречаются в 4% случаев [72]. Ротационные вывихи характеризуются невозможностью их закрытого вправления.
Также считаем целесообразным еще раз остановиться на терминологических коллизиях. Когда речь идет о способах лечения повреждений связок, то используются термины реконструкция (англ. reconstruction) и восстановление (англ. repair). Конечно же, филологически эти термины обозначают одно и то же, но на практике реконструкция подразумевает использование ауто- или аллотрансплантата, а восстановление – сшивание поврежденной структуры.
Первичная оценка острых и хронических множественных повреждений связок коленного сустава
Первичная оценка пациента со свежими или застарелыми множественными повреждениями связок коленного сустава производится посредством тщательного и полного обследования нейроваскулярного статуса, состояния мягких тканей и определения характера нестабильности. Особенно важно оценить состояние сосудов, так как их повреждение может привести к катастрофической дисфункции конечности и, в конечном итоге, к ампутации. Травма большеберцового и/или малоберцового нерва также может иметь разрушительные последствия и встречается почти в 25% вывихов голени [50]. Для описания подобного рода травм широко используется классификация R.C. Schenck (Таблица 1) [57, 58, 59] и модификация этой классификации D.C. Wascher (Таблица 2) [73], в которой учитывается не только связочный аппарат, но повреждения сосудисто-нервного пучка и околосуставные переломы.


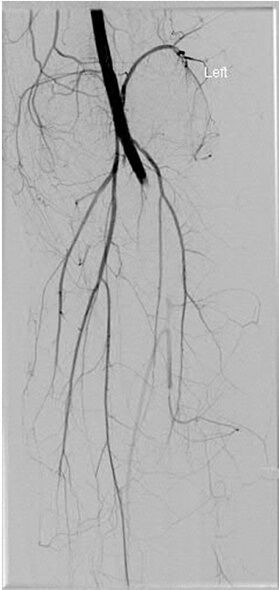
Существует несколько алгоритмов обследования сосудистого статуса нижней конечности. Васкулярное обследование может включать сам осмотр, оценку лодыжечно-плечевого индекса (ЛПИ), ультразвуковое исследование артерий и стандартную и/или компьютерную томографическую ангиографию. За счет коллатерального кровотока даже при полной окклюзии подколенной артерии может сохраняться пульсация дистальных артерий (Рисунок 1). Когда у пациента присутствуют «тяжелые признаки» ишемии, такие как холодная, лишенная пульсации, явно некровоснабжаемая нижняя конечность, необходима немедленная консультация сосудистого хирурга. Если известен уровень повреждения (например, подколенная артерия при вывихе голени в коленном суставе), сосудистый хирург может предпочесть немедленную диагностическую операцию или провести ангиографию. Как правило, для восстановления кровотока используют обходное шунтирование подкожной веной (v. saphena), взятой с контралатеральной стороны, и выполняют профилактическую четырехкомпартментную фасциотомию. Когда у пациента присутствуют «легкие признаки» ишемии, такие как пальпируемый, но ассиметричный пульс, а также ассиметричные тепловые или цветовые характеристики нижней конечности, необходимо дополнительное обследование.
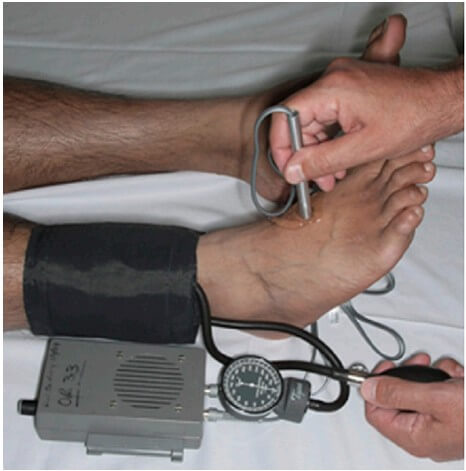
Лодыжечно-плечевой индекс (ЛПИ) определяется посредством измерения систолического давления крови пораженной конечности на уровне лодыжек (Рисунок 2), систолического давления крови ипсилатеральной руки на уровне плечевой артерии и вычисляется по формуле:
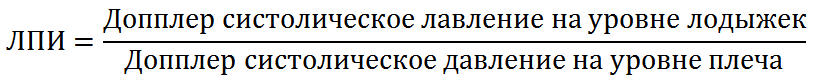
Mills и соавторы показали [46], что если ЛПИ≥0,9, то повреждения магистральной артерии нет, но из-за сохраняющегося риска тромботических осложнений необходимо в течение суток измерять пульс каждые 4-6 часов. Если ЛПИ<0,9, то необходимо выполнить или ультразвуковое исследование артериальное, или компьютерную томографическую ангиографию [42]. Дуплексное артериальное ультразвуковое исследование имеет великолепную чувствительность и специфичность, но, тем не менее, ее результаты во многом зависят от технической оснащенности и мастерства специалиста, и не у всех лечебных учреждений имеется круглосуточная возможность выполнить это исследование. Преимуществом компьютерной томографической ангиографии перед обычной ангиографией является то, что пациент доза облучения снижается более чем в 4 раза, доступ осуществляется через локтевую ямку, а не через пах, а чувствительность и специфичность приближаются к 100% [52]. У стандартной ангиографии частота ложно-положительных результатов составляет 5-7%.
Нейрологическое обследование
Niall и соавторы [50] сообщили, что при вывихе в коленном суставе частота повреждений малоберцового нерва составляет около 25%. По их данным восстановление функции нерва имело место у менее чем половины пациентов. В таких случаях для профилактики эквинусной деформации ввиду некомпенсированной тяги трехглавой мышцы голени необходимо в раннем посттравматическом периоде накладывать ортез, иммобилизирующий стопу в плантиградном положении.
Лечение пациентов с посттравматическим параличом малоберцового нерва может состоять из пластики икроножного нерва, непосредственного сшивания по типу «конец-в-конец», невролиза и транспозиции большеберцовых сухожилий, но, к сожалению, успех таких вмешательств весьма вариабелен. Многообещающим направлением видится прямая транспозиция двигательных ветвей большеберцового нерва к малоберцовому нерву, но отдаленные результаты этой процедуры не известны.
Визуализирующие методы исследования
Как мы уже отмечали, весьма часто вывихи голени вправляются самостоятельно, и, соответственно, рентгенологическая картина может быть непоказательной. Тем не менее, обязательно выполнение стандартных рентгенограмм в переднезадней и боковой проекциях. Асимметрия сустава, небольшой большеберцово-бедренный подвывих, оскольчатые, отрывные и краевые переломы дают важную информацию о характере травмы связочного аппарата. При отсутствии острой клинической ситуации в определении степени нестабильности коленного сустава может помочь билатеральная сравнительная функциональная стресс-рентгенография (с варусным, вальгусным и задним форсированным отклонением голени).
LaPrade и соавторы [34] сообщили, что асимметрия в боковом отклонении голени более чем на 2,7 мм при варусной стресс-рентгенографии в переднезадней проекции указывает на повреждение малоберцовой (латеральной) коллатеральной связки коленного сустава, а асимметрия более 4 мм свидетельствует о травме латеральной коллатеральной связки и повреждении заднелатерального угла. При острой клинической ситуации возможно проведение флуороскопического функционального обследования пациента под анестезией.
Магнитно-резонансная томография является предпочтительным методом диагностической визуализации после получения рентгенограмм. Магнитно-резонансная томография позволяет идентифицировать локализацию и степень повреждения связок, что исключительно важно для планирования хирургического вмешательства.
Показания к экстренному хирургическому вмешательству
Показаниями к экстренному хирургическому вмешательству являются: открытый вывих в коленном суставе, невправимый вывих и компартмент-синдром. Открытый вывих колена требует проведения тщательной санации в виде ирригации и дебридмента, возможно использование цементных бус с антибиотиком и/или наложения вакуумной повязки (VAC). В случае дефекта покровных тканей может потребоваться реконструктивная операция по закрытию раны. Невправимый вывих колена – это, обычно, ротационный заднелатеральный вывих, при котором медиальный мыщелок бедренной кости проходит через медиальную поверхность капсулы и/или медиальную коллатеральную связку по типу «пуговица в петлю», когда можно увидеть классическую картину натяжение кожи по медиальной стороне колена. Во избежание некроза покровных тканей в таких случаях необходима экстренная репозиция, которая часто возможна только артротомическим путем. При экстренной операции полноценная реконструкция связочного аппарата нецелесообразна, важно создать благоприятные условия для последующей этапной реконструкции, направив основные усилия на санацию, дебридмент и успешное заживление раны. Если выполнено сосудистое шунтирование, и/или, если вывих был открытым, а также в тех случаях, когда вправление нестабильно и имеется тенденция к повторному вывиху или подвывиху, то показано наложение аппарата внешней фиксации [38, 40].
Сочетанное повреждение задней и передней крестообразных связок
Принципы лечения сочетающихся повреждений передней и задней крестообразных связок в себя тщательную диагностику, правильный выбор времени операции, точное воссоздание биомеханических векторов нативных связок путем адекватного формирования каналов для трансплантатов в местах анатомического (физиологического) ранее поврежденных связок; использование качественных, механически прочных трансплантатов; их надежная фиксация и грамотную программу послеоперационной реабилитации [7, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 22, 23, 38, 39].
G.C. Fanelli и соавторы [21] при однопучковой реконструкции задней крестообразной связки колена предпочитают использовать аллотрансплантант ахиллова сухожилия. При двухпучковой реконструкции задней крестообразной связки те же авторы рекомендуют использовать аллотрансплантаты ахиллова сухожилия и сухожилия передней большеберцовой мышцы. Для реконструкции передней крестообразной связки авторы предпочитают использовать аллотрансплантаты сухожилия передней большеберцовой мышцы или связки надколенника. В ходе стабилизации артроскоп вводят через нижнелатеральный парапателлярный портал, а инструменты вводят через нижнемедиальный портал, что позволяет лучше контролировать локализацию туннелей на бедренной кости. Для защиты нейрососудистых структур и для контроля правильности позиционирования тибиального канала в ходе операции выполняется дополнительный внесуставной задневнутренний портал.
Сначала выполняется подготовка мест прикрепления трансплантатов (notch-пластика межмыщелковой вырезки), состоящая из резекции культей задней и передних крестообразных связок, формирования латеральной, медиальной стенок и крыши межмыщелкового пространства. Для визуализации места прикрепления задней крестообразной связки к большеберцовой кости используют специальные кюретки и распаторы и изгибом рабочей части по углом в 90 градусов, которые заводят сквозь вырезку к задней части суставной поверхности большеберцовой кости. Этими инструментами отсепаровывают мягкие ткани и приподнимают капсулу.
Кронштейн направителя задней и передней крестообразных связок заводят нижнемедиальный портал. Сначала формируют тибиальный канал для задней крестообразной связки. Конец направителя размещают в нижнелатеральной части поверхности анатомического прикрепления задней крестообразной связки. Упор направителя контактирует с переднемедиальной поверхностью проксимальной части большеберцовой кости в точке, располагающейся посередине между заднемедиальной границей и передней границей большеберцового плато, примерно, на 1 см ниже бугристости большеберцовой кости. Это положение дает возможность сориентировать трансплантат под углом в 45 градусов к задней части поверхности большеберцовой кости, а не изгибать его под прямым углом, что может вызвать некроз вследствие сдавливания трансплантата.
Положение верхушки направителя в задней части поверхности большеберцовой кости контролируется пальцем хирурга через внекапсулярный задневнутренний дополнительный разрез. Целесообразно выполнить интраоперационную рентгенографию в передне-задней и боковой проекциях, которые помогут оценить правильность локализации направителя. По направителю заводят спицу, при этом хирург продолжает контролировать пальцем через заднемедиальный портал место ее выхода. Далее формируют стандартными канюлированными фрезами большеберцовый канал соответствующего диаметра. Хирург продолжает контролировать пальцем положение направительной спицы для правильного формирования канала. Сверло продвигают до заднего кортекса большеберцовой кости, затем дрель отсоединяют от сверла, и формирование большеберцового канала завершают вручную, что снижает риск повреждения нейрососудистых стуктур.
Бедренные каналы для однопучковой или двухпучковой реконструкции задней крестообразной связки могут быть выполнены изнутри наружу. Введение двухпучкового направителя соответствующего размера через нижний медиальный портал позволяет сформировать бедренный канал для переднебокового пучка трансплантанта задней крестообразной связки. Двухпучковый напраитель размещают непосредственно в месте прикрепления переднебокового пучка задней крестообразной связки к бедренной кости. Сверлят канал спицей, выводя ее наружу через дополнительный разрез на коже. Двухпучковый направитель вынимается и, под артроскопическим контролем, окончательно формируют бедренный канал переднебокового пучка трансплантата задней крестообразной связки фрезой соответствующего диаметра по направлению изнутри-наружу. Если хирург выполняет двухпучковую реконструкцию задней крестообразной связки с формированием двойного бедренного канала, такая же процедура повторяется для заднемедиального пучка трансплантата задней крестообразной связки. Между двумя каналами в бедренной кости должно быть не менее 5 мм.
Каналы для однопучковой реконструкции передней крестообразной связки выполняются через один разрез. Тибиальный канал начинается снаружи в 1 см проксимальнее бугристости большеберцовой кости на переднемедиальной поверхности проксимальной части большеберцовой кости и заканчивается в центре места прикрепления передней крестообразной связки к большеберцовой кости. Бедренный канал формируют в латеральном мыщелке бедренной кости рядом с анатомическим местом крепления передней крестообразной связки. Трансплантат передней крестообразной связки размещают и фиксируют в бедренном канале, затем трансплантата натягивают и фиксируют в большеберцовом канале (Рисунок 3-Рисунок 5) [25].
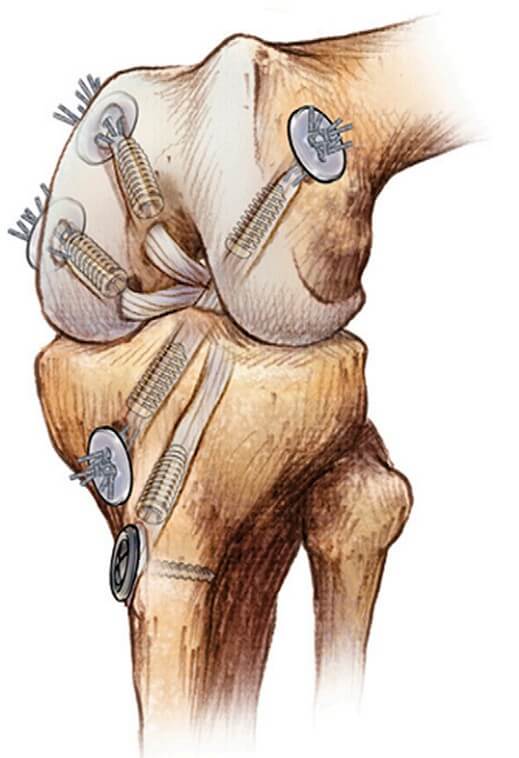
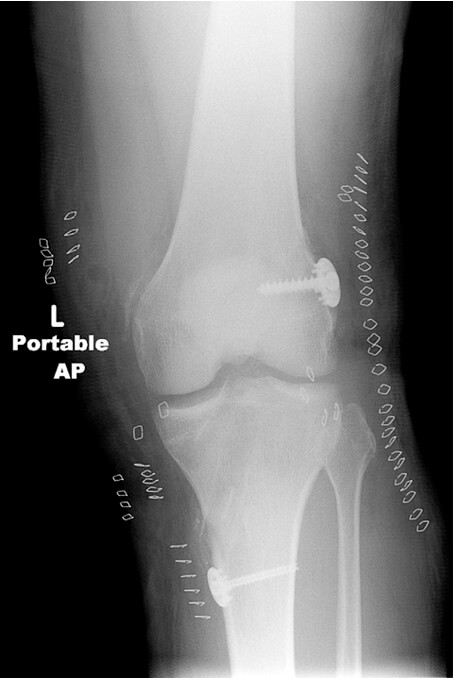
Латеральная реконструкция
При вывихах в коленном суставе латеральные связочные структуры повреждаются практически всегда, и, такие повреждения являются составной частью мультисвязочных повреждений. Классификация вывихов в коленном суставе R.C. Schenck [57, 58, 59] в модификации D.C. Wascher [73] включает в себя рубрику KD IIIL (повреждение передней, задней крестообразных связок и бокового комплекса). Вариант повреждения KD IV (повреждение обеих крестообразных связок, латерального и медиального комплекса) является менее распространенным и более тяжелым. Механизм этой травмы характеризуется значительным высокоэнергетическим варусным отклонением и наружной ротацией голени [58]. Латеральный комплекс связок коленного сустава имеет сложную анатомию, что обуславливает значительные трудности при реконструкции.
Латеральный комплекс сторона состоит из статичных и динамических стабилизаторов коленного сустава. Статичные стабилизаторы включают в себя малоберцовую коллатеральную связку, подколенно-малоберцовую связку, а также заднелатеральную суставную капсулу. Подколенные мышца и сухожилие действуют одновременно как статичные и динамические стабилизаторы, контролирующие заднелатеральную ротацию голени. Малоберцовая коллатеральная связка выступает как первичный ограничитель варусного отклонения и вторичный ограничитель заднелатеральной ротации большеберцовой кости по отношению к бедренной кости. Подколенно-малоберцовая связка выступает как первичный ограничитель наружной ротации большеберцовой кости по отношению к бедренной кости при сгибании колена на 30 градусов. Такую же функцию выполняют подколенная мышцей и ее сухожилие. Заднелатеральная капсула играет второстепенную вспомогательную роль при сопротивлении наружной ротации, перерастяжению и варусному отклонению [1, 36, 55].
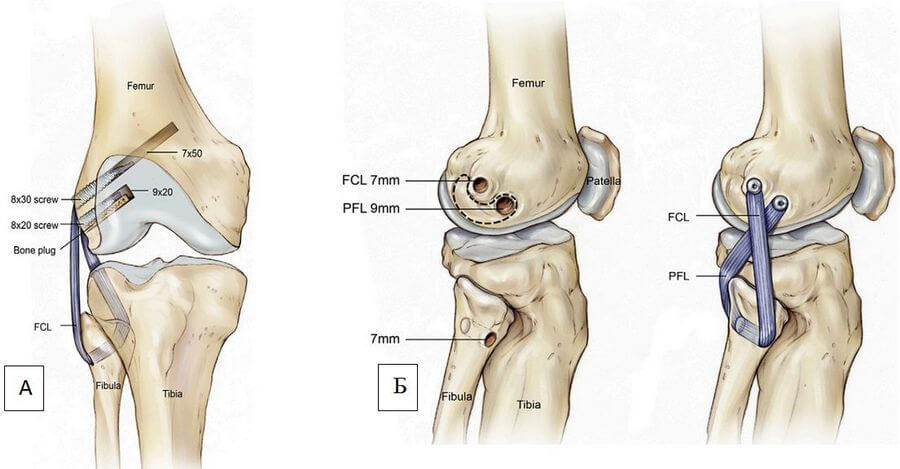
Реконструкция должна быть максимально анатомической, что позволит наиболее полноценно воссоздать биомеханику нативных связок. Для этого формируют комбинированные каналы в бедренной, большеберцовой и малоберцовой костях, а в качестве трансплантата используют алломатериалы. Альтернативой является упрощенная, неполная реконструкция заднелатеральных структур с формированием каналов только в бедренной и малоберцовых костях (фибуло-феморальная реконструкция, Рисунок 6) [17, 19, 49, 56, 60]. Имеется лишь несколько исследований, сравнивающих типы реконструкций, однако логично предположить, что наилучшие результаты возможны при анатомических вариантах. Реконструкция, описанная LaPrade и соавторами [35], часто рассматривается как наиболее близкое воспроизведение нормальной анатомии.
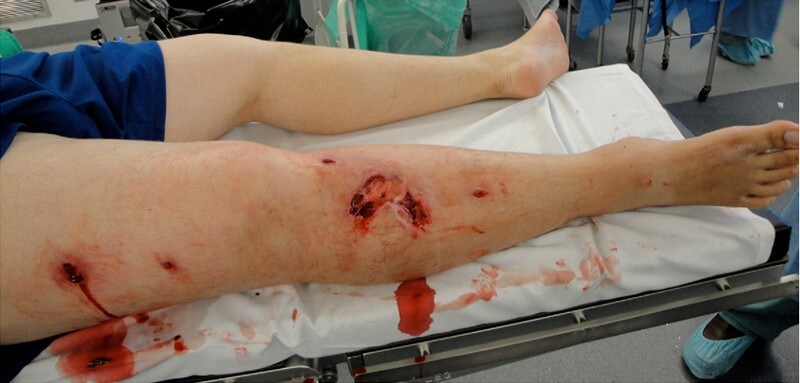
Время проведения хирургической стабилизации всегда было одним из наиболее спорных аспектов лечения вывихов в коленном суставе. Последние исследования показывают [64], что более ранняя реконструкция может дать лучшие результаты, но уровень доказательности этого утверждения пока невысок. Достоинства раннего хирургического вмешательства противопоставляются риску артрофиброза и инфекционных осложнений в случае поврежденных или скомпрометированных покровных тканей как в результате самой травмы, так и в результате первичного открытого вправления либо использования аппаратов внешней фиксации (Рисунок 7). Решение о сроке проведения оперативного вмешательства должно приниматься в индивидуальном порядке.
Еще один спорный вопрос заключается в выборе между восстановлением (сшивание поврежденных связок) и реконструкцией (пластикой) заднелатерального угла. Последние исследования Stannard и соавторов [64], Levy и соавторов [37] указывают на то, что, вероятнее всего, реконструкция лучше восстановления. Если оперативное вмешательство проводится в срок не позднее 3-х недель после травмы, то возможно комбинированное проведение восстановления и реконструкции, что, вероятно, даст лучшие результаты по стабилизации заднелатерального угла [21]. Недавно Stannard и соавторы [64] сообщили о результатах исследования, сравнивающего восстановление заднелатерального угла с реконструкцией у 57 пациентов. У 44 (77%) пациентов имелись множественные травмы связок коленного сустава, а минимальная продолжительность послеоперационного наблюдения составила 24 месяца. Частота неудачного восстановления составила 37% против 9% при проведении реконструкции. Таким образом, реконструкция оказалось более предпочтительной по сравнению с восстановлением в плане стабильности.
В проспективном исследовании, проведенном Levy и соавторами [37], пациенты с множественными травмами связок коленного сустава проходили лечение у одного и того же хирурга. В период между февралем 2004 и маем 2005 года пациентам проводились процедуры по восстановлению медиальных и латеральных стабилизирующих структур, после чего, вторым этапом, были проведены отсроченные реконструкции крестообразных связок коленного сустава. В период между маем 2005 и февралем 2007 года, пациентам выполняли одноэтапные реконструкции всех поврежденных связок. Результаты лечения 44 пациентов (45 суставов) были прослежены в течение минимум 2 лет. 4 из 10 случаев восстановления малоберцовой коллатеральной связки и заднелатерального края, а также 1 из 18 случаев реконструкции малоберцовой коллатеральной связки и заднелатерального края закончились неудачно (р=0,04). Хотя оба эти исследования не были рандомизированными, они показали схожие результаты, заключающиеся в том, что частота неудачных попыток восстановления малоберцовых коллатеральных связок значительно выше частоты их неудачных реконструкций.
Для лечения повреждений заднелатерального угла предлагалось большое число различных вариантов хирургического лечения, показавших неоднородные клинические результатами [17, 65, 69, 76]. Stannard и соавторы [65] применяли модифицированную двухпучковую технику, которая реконструирует подколенно-малоберцовую связку связки и малоберцовую коллатеральную связку: трансплантат проводят через каналы в большеберцовой и малоберцовых костях и с помощью одного винта фиксируют на латеральном мыщелке бедра. На протяжении минимум 2 лет были прослежены результаты лечения 22 пациентов. Средняя амплитуда движений на конечном этапе наблюдения составила 133 градуса, а среднее значение по шкале Lysholm составило 90 баллов для всех пациентов, 92 баллов для случаев множественных травм связок, и 88 баллов при проведении изолированной реконструкции заднелатерального угла. Было 2 случая неудачной стабилизации (13%) в группе с множественными травмами связок, а при изолированной реконструкции заднелатерального угла случаев неудач не было.
Strobel и соавторы [69] оценили клинические результаты через 2 года после одноэтапных реконструкций передних крестообразных и задних крестообразных связок, а также заднелатерального угла у 17 пациентов. Заднелатеральный угол был реконструирован при помощи трансплантата, проходящего через проксимальную часть малоберцовой кости, со вставкой обоих ножек трансплантата в изометрической точке на бедренной кости. При финальной оценке, проведенной при помощи шкалы IKDC, близкие к нормальным результаты были получены у 5 из 17 пациентов, ниже нормальных — у 10, и как недопустимые — у 2. Средний субъективный результат по шкале IKDC составил 71,8±19,3 баллов.
Оперативная техника (процедура) LaPrade [35] популяризировалась как стабильная и анатомически полная реконструкция с использованием двухпучкового аллотрансплантата (обычно ахиллова сухожилия), восстанавливающая биомеханические вектора малоберцовой коллатеральной связки, подколенно-малоберцовой связки и подколенного сухожилия. Для данной техники необходимы четыре канала: два в бедренной кости (для крепления трансплантата коллатеральной связки и подколенного сухожилия), один в большеберцовой кости и еще один – в проксимальной части малоберцовой кости. Ахиллово сухожилие может быть разделено на 2 отдельных трансплантата с костными блоками. Оба костных блока вставляются в бедренные каналы соответственно местам прикрепления коллатеральной связки и подколенного сухожилия и фиксируются интерферентными винтами. Пучок трансплантата, реконструирующий малоберцовую коллатеральную связку, проходит спереди назад через канал в малоберцовой кости, а затем и в большеберцовой кости. Затем следует пучок, реконструирующий подколенное сухожилие: он направляется от бедренной кости к тибиальному туннелю, где он встречается с первым пучком трансплантата. После натяжения трансплантатов в положении сгибания колена под углом в 30 градусов и легкой внутренней ротации голени выполняют фиксацию пучков трансплантата интерферентным винтом, который вводят спереди назад. Слишком сильная ротация внутрь может послужить причиной контрактуры коленного сустава. Эта операция технически сложна, но позволяет получить хорошие результаты (Рисунок 8).
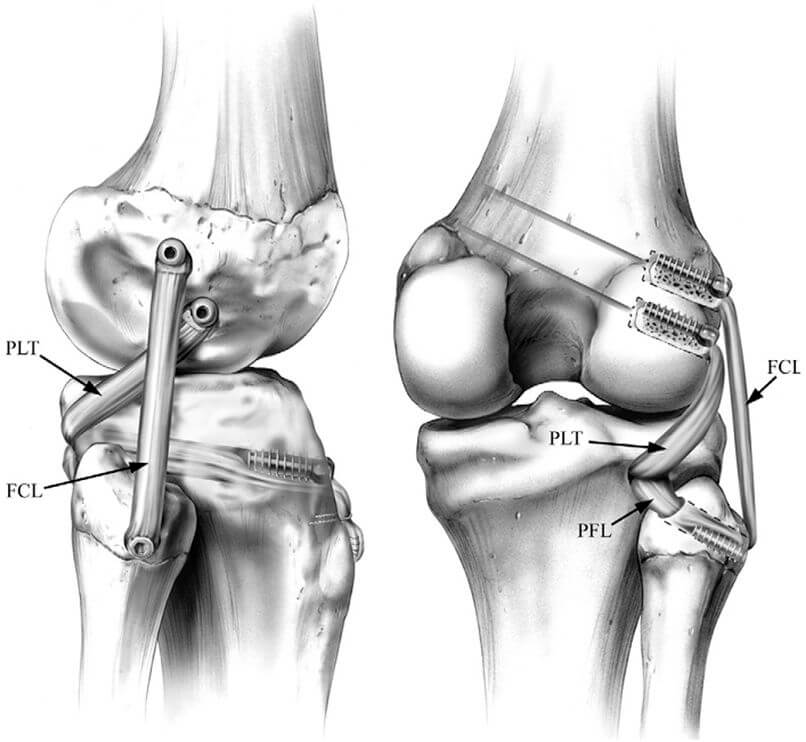
Если поврежден заднелатеральный угол, то обычно имеются повреждения и других связок (малоберцовая коллатеральная связка, подколенно-малоберцовая связка), которые также необходимо реконструировать. Для таких реконструкций предпочтительно использовать аллотрансплантаты, что исключает морбидность донорского места [21]. Существует много вариантов стабилизации, но, конечно же, наилучшие результаты возможны при применении той методики, которой владеет хирург.
Реконструкция медиальной коллатеральной связки и заднемедиального края
Комбинированные повреждения передней, задней крестообразных связок и медиальной коллатеральной связки/заднемедиального угла относятся к III по классификации R.C. Schenck [57, 58, 59] в модификации D.C. Wascher [73]. Анатомические структуры медиальной части разделены на 3 слоя: первый слой – портняжная мышца и портняжная фасция; второй слой – поверхностная медиальная коллатеральная связка, задняя косая связка и полуперепончатая мышца; третий слой – глубокая медиальная коллатеральная связка (мениско-бедренная и мениско-большеберцовая связки) и заднемедиальная часть капсулы. Сухожилие нежной и полусухожильной мышц располагаются между первым и вторым слоем. Эти слои не всегда отделены друг от друга, т.к. первый и второй слои соединяются спереди, а второй и третий соединяются сзади.
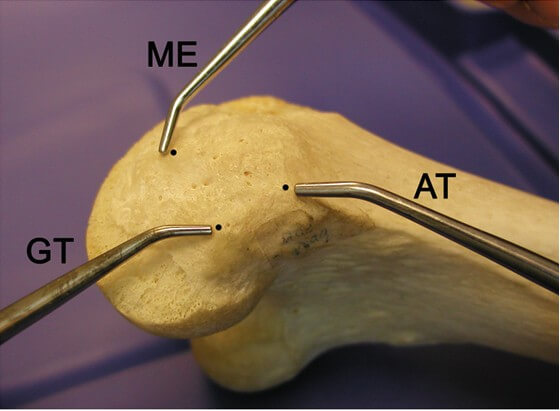
LaPrade и соавторы [33] описали клиническую анатомию медиальных структур коленного сустава. На дистальной части бедренной кости имеется 3 костных выступа: медиальный надмыщелок, приводящий бугорок бедренной кости и икроножный бугорок (Рисунок 9). Прикрепление к бедренной кости поверхностной медиальной коллатеральной связки локализуется примерно в 3 мм проксимальнее и в 5 мм кзади от надмыщелка, при этом место крепления к большеберцовой кости располагается примерно на 6 см дистальнее линии сустава. Глубокая медиальная коллатеральная связка крепится вдоль края плато большеберцовой кости, чуть дистальнее суставного хряща. Прикрепление задней косой связки к бедренной кости располагается примерно в 8 мм дистальнее и в 6 мм кзади от приводящего бугорка. Эти анатомические образования соответствуют рентгенографическим ориентирам, описанным Wijdicks и соавторами [74]. Stannard и соавторы [67] выяснили, что именно применение рентгенографических ориентиров, а не пальпация приводят к лучшей репродукции изометрии поверхностной медиальной коллатеральной связки. Тем не менее, комбинация интраоперационной оценки локализации этих бугорков с рентгенологической картиной помогает хирургу правильно сориентировать места начала и прикрепления пучков трансплантата.
Раскрытие более чем на 10 мм медиальной суставной щели при выполнении вальгусного стресс-теста при полном разгибании голени является отличительным признаком комбинированной травмы колена с поражением медиального комплекса связок и обеих крестообразных связок. Стресс-тесты должны выполняться под анестезией, а результат должен оцениваться по рентгенограмме в сравнении с контрлатеральным неповрежденным коленным суставом.
При условии, что покровные мягкие ткани находятся в удовлетворительном состоянии, хирургическая стабилизация выполняется через 1-3 недели после травмы. В такие сроки операция выполняется при обширном медиальном повреждении, разрыве мениска со смещением или, так называемом, повреждении Stener, при котором дистальная часть медиальной коллатеральной связки обворачивается вокруг сухожилий в области «гусиной лапки». Отсроченное оперативное вмешательство (в срок более чем через 3 недели после травмы) может быть показана в тех случаях, когда имеется посттравматический отек, затрудняющий движения в коленном суставе. Если единственным повреждением медального комплекса является повреждение медиальной коллатеральной связки, то возможно ее самостоятельное сращение, и в таком случае, проводится реконструкция только крестообразных связок. Когда необходимо реконструировать переднюю и заднюю крестообразные связки, медиальный комплекс оптимальна одноэтапная реконструкция, в ходе которой, по показаниям, выполняют реконструкцию и заднемедиального угла.
В экстренных случаях авульсивный отрыв медиальной коллатеральной связки от бедренной или большеберцовой кости может быть выполнена рефиксация винтом с накладкой. В таких случаях связка на своем протяжении за исключением места прикрепления оказывается практически интактной, что позволяет выполнить только лишь рефиксацию без каких-либо пластических мероприятий (Рисунок 10). При этом глубокая мениско-бедренная связка может быть рефиксирована с помощью якорей. Реконструируемые связки необходимо натянуть в положении сгибания в коленном суставе на 30 градусов, варусном отклонении и небольшой ротации голени наружу, после чего выполняется фиксация. Поврежденные заднюю косую связку и заднемедиальную капсулу реконструируют анатомически посредством сшивания в натяжении при почти полном разгибании голени. Очень важно не допустить излишнего натяжения при сгибании в коленном суставе, т.к. это может препятствовать полному разгибанию.
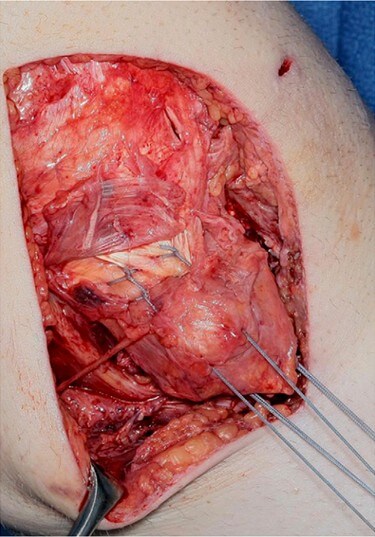
Для лечения застарелых разрывов предлагалось несколько вариантов хирургического лечения [3, 22, 32, 43]. G.C. Fanelli [21] рекомендует использовать аллотрансплантаты ахиллова сухожилия с костным блоком, который фиксируется в мыщелке бедренной кости интерферентным винтом (Рисунок 11), а сухожильная часть фиксируется в большеберцовой кости накостными приспособлениями (накладки, шайбы и др.). Задняя косая связка и заднемедиальная капсула восстанавливаются по показаниям.
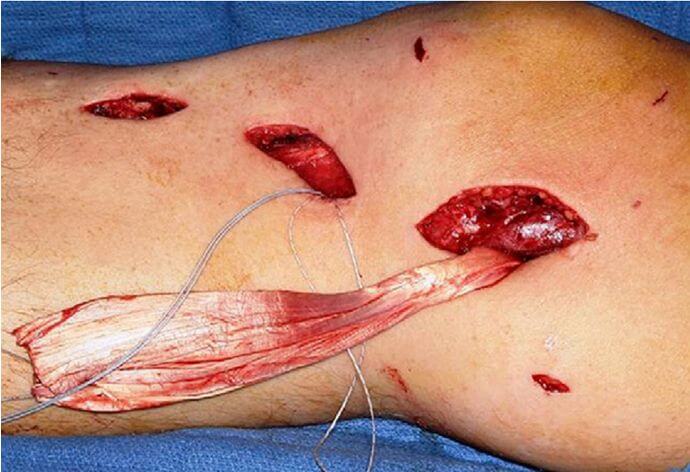
Специализированный поиск литературы за период с 1978 по 2008 гг. по результатам восстановления или реконструкции медиальной коллатеральной связки при множественных повреждениях связок коленного сустава [38] показал, что только 8 работ отвечают критериям включения. Пять из них были посвящены восстановлению медиальной коллатеральной связки, и три – реконструкции медиальной коллатеральной связки. Проспективных исследований, непосредственно сравнивающих консервативное и оперативное лечение при повреждениях медиальной коллатеральной связки, а также сравнивающих реконструкцию и восстановление, не было. Обобщенные результаты предполагают, что как восстановление, так и реконструкция при множественных травмах позволяют получить удовлетворительные результаты.
Owens и соавторы [51] сообщили о результатах лечения 11 пациентов с повреждениями передней, задней крестообразных связок и медиальной коллатеральной связки. Последнюю авторы восстанавливали только в том случае, если она была повреждена полностью. Во всех случаях стабилизация была успешной и вальгусный стресс-тест был отрицательным. G.C. Fanelli и соавторы [20] сообщили о 9 случаях повреждений передней, задней крестообразных связок и медиальной коллатеральной связки. В 7 случаях выполнялась хирургическая стабилизация. У всех девяти пациентов коленный сустав оказался стабильным, а вальгусный стресс-тест – отрицательным. В работе Hayashi и соавторов [28] 7 случаев реконструкции передней, задней крестообразных связок и медиальной коллатеральной связки выполнялись аутотрансплантата полусухожильной мышцы. Результаты по шкале Lysholm составили 95.1 баллов. Stannard и соавторы [67] сделали отчет по 73 клиническим случаям вывихов голени с повреждением заднемедиального угла. В 28 случаях для реконструкции медиальной коллатеральной связки использовались ауто- или аллотрансплантаты, а у 24 пациентов выполнялось восстановление медиальной коллатеральной связки. В группе восстановления частота неудач составила 20% по сравнению с 4% в группе реконструкции.
Ключевыми моментами лечения пациентов с множественными повреждениями связок, включающими в себя повреждение медиального комплекса, являются точная диагностика на основе как клинических данных, так и результатов визуализирующих методов исследования, стресс-рентгенограмм; правильный выбор времени операции и хирургической тактики: реконструкция передней, задней крестообразных связок, восстановление или реконструкция медиальной коллатеральной связки, задней косой связки и заднемедиальной капсулы.
Послеоперационная реабилитация
Колено должно находиться в полностью разогнутом состоянии в течение минимум трех недель после операции. Осевая нагрузка исключается в течение 6 недель [29]. Через 3 недели после операции начинают делать упражнения с нарастающей амплитудой движения. При этом пациент продолжает носить брейс, ограничители которого регулируются с постепенным увеличением амплитуды. Полная осевая нагрузка возможна по принципу толерантности: т.е. от костылей отказываются тогда, когда пациент сможет опереться на ногу. Продолжают выполнять упражнения с закрытой кинематической цепью по прогрессивному типу. Ортез снимают через 10 недель после операции. Пациент может вернуться к занятиям спортом и интенсивной работе через 9 месяцев после операции, когда в достаточной мере будут восстановлены сила и амплитуда движений [7 24]. После стабилизации по поводу множественных повреждений связок коленного сустава можно ожидать потерю 10-15 градусов сгибания [21].
Переломовывихи
Переломовывихиколенного сустава, несомненно, тяжелая травма, а результаты лечения таких пациентов часто разочаровывают [2, 6, 30, 47, 48, 68]. Среди всех многообразных вариантов околосуставных переломов, сочетающихся с множественными повреждениями связок, наиболее часто встречаются переломы плато большеберцовой кости. Лечение таких пациентов – трудная задача, поскольку нестабильность вызвана как повреждением связок, так и переломом. Порочный круг нестабильности иллюстрируют исследования, которые показали, что частота неудач раннего лечения пациентов с повреждением заднелатерального угла путем реконструкции двухпучковым способом хуже, если у пациента имеется перелом верхней суставной поверхности большеберцовой кости [64, 65].
На самом деле переломовывихи коленного сустава встречаются чаще, чем считается, что подчеркивает сложность диагностики таких повреждений. Действительно, в том случае, если у пациента имеется перелом плато большеберцовой кости тесты нестабильности при повреждениях связок весьма затруднительны. Кроме того, часто это пациенты с политравмой, затрагивающей и другие анатомические области, что еще более усугубляет сложность диагностики. Стоит отметить, что исследования с использованием магнитно-резонансной томографии показали, что частота повреждений связок при переломе плато большеберцовой кости варьирует от 33% до 90% [26, 31, 61, 66]. В этих исследованиях не все клинические случаи были переломовывихами, в связи с чем представляют интерес данные Stannard и соавторов [66], которые показали, что из 103 пациентов с околосуставным переломом плато большеберцовой кости у 52 пациентов имелись повреждения более чем одной связки, а у 27 – был истинный переломовывих. Для диагностики сочетающихся повреждений кости и связочного аппарата целесообразно использовать визуализирующие методы исследования (рентгенография, ультрасонография, и, при возможности, магнитно-резонансная томография) под анестезией.
Существует лишь небольшое количество исследований по лечению переломовывихов коленного сустава. Опубликованные результаты показывают высокую частоту неудовлетворительных результатов, обусловленных болью, нестабильности и артрофиброзом [2, 6, 30, 47, 48, 68]. Консервативное лечение дает еще более худшие результаты, в связи с чем большинство авторов рекомендует оперативное лечение таких пациентов. Delamarter и соавторы [5] сообщили, что 40% их пациентов с переломовывихами имели неудачный исход заболевания после консервативного лечения по сравнению с 16% неудовлетворительных результатов у прооперированных пациентов. Stannard и соавторы [62] разработали этапный протокол лечения пациентов с переломовывихами, в котором лечение перелома отделяется от лечения вывиха, что позволило получить хороший функциональный исход у большинства пациентов.
Первый этап лечения пациента с переломовывихом коленного сустава начинается в день получения травмы. Изучают анамнез, механизм травмы, на основе данных осмотра и рентгенографии ставят предварительный, неуточненный диагноз переломовывиха, и выполняют репозицию. На протяжении всего первого этапа лечения важно контролировать состояние сосудов и нервов с четким документированием возможных повреждений в истории болезни. Если после репозиции удалось получить конгруэнтный сустав, то накладывают иммобилизацию, после чего выполняют магнитно-резонансную томографию, позволяющую получить уточненный диагноз. В большинстве случаев переломовывихов повреждены или скомпрометированы покровные ткани, что делает невозможным срочное хирургическое лечение, которое нужно отложить до спадения отека и нормализации состояния покровных тканей.
Второй этап лечения состоит в хирургической стабилизации перелома и любых повреждений главных связок. Для околосуставных переломов целесообразно использовать пластины с принципом блокирующих винтов. Предоперационное планирование должно быть очень тщательным, чтобы винты не мешали формированию каналов для последующей реконструкции связок. Интраоперационно важно удостоверится в том, что нет вывиха или подвывиха, а после операции накладывают иммобилизацию.
Третий этап лечения – это ранняя реконструкция связочного аппарата, к которой приступают, как правило, через 3-4 недели после травмы. Основа этого этапа – реконструкция связок аллотрансплантатами. В литературе нет однозначных данных о том, когда должен начинаться реконструктивный этап и также о самой этапности реконструкций при переломовывихах. Stannard и соавторы [64, 65] считают, что реконструкция передней крестообразной связки и заднелатерального угла должна выполняться приблизительно через 4 месяца после травмы, что позволит срастись перелому плато большеберцовой кости для безопасного формирования тибиальных туннелей трансплантатов. По их данным частота неудачных исходов превышает 30% в том случае, если реконструкция заднелатерального угла выполнялась на третьем этапе лечения по сравнению с 8% неудач, если та же реконструкция заднелатерального угла выполнялась у пациентов после сращения перелома плато большеберцовой кости [64, 65]. Сразу после хирургической стабилизации сустава накладываю шарнирный наружный фиксатор (брейс), что создает благоприятные условия для приживления трансплантата. Если позволяет состояние мягких тканей, то шарниры брейса освобождают на следующий день после операции таким образом, чтобы разрешить движения с небольшой амплитудой.
Четвертый этап лечения – это поздняя реконструкции. К ней приступают в том случае, если амплитуда движений в коленном суставе составляет как минимум 80% от нормальной. Брейс снимают и оценивают стабильность коленного сустава: реконструкцию передней крестообразной связки и заднелатерального угла выполняют в том случае, если имеется клинически значимая нестабильность. Для пластики связок G.C. Fanelli и соавторы рекомендуют использовать аллотрансплантаты [21]. В любом случае, иммобилизация в послеоперационном периоде не должна быть жесткой, чтобы минимизировать риск артрофиброза.
По данным Stannard и соавторов [62], хороший функциональный исход лечения пациентов с переломовывихами достигался как раз при использовании этапного подхода. Результаты этапного лечения 50 пациентов с 54 переломовывихами составили 86 баллов по шкале Lysholm (от 50 до 100 баллов). Результаты лечения по шкале IKDC показали 32 случая нормальных или почти нормальных коленных сустава и 17 – не соответствующих норме. Стоит отметить, что для достижения этих результатов каждому пациенту в среднем было выполнено по 4 четыре операции для исчерпывающей реконструкции.
Осложнения
К сожалению, вывихам и переломовывихам часто сопутствуют различные осложнения, обусловленные как самой травмой, так и сложностью лечения. Осложнения включают в себя проблемы с заживлением раны (как при открытом вывихе, так и при сдавлении мягких тканей смещенной костью, послеоперационные раны), сосудистые и неврологические проблемы. Наиболее частыми осложнениями лечения являются боль, артрофиброз и нестабильность реконструированного сустава. Боль трудно поддается объективной оценке, но многие пациенты страдают хроническими болями после получения таких травм: по данным исследователей частота хронической боли варьирует от 25 до 86% [63]. Артрофиброз, который также может служить и причиной болей, возникает в по данным литературы возникает в 5-71% случаев, а хирургическое лечение по поводу этого осложнения требуется в 29% (от числа всех пациентов с артрофиброзом) [63]. Частота нестабильности по данным J. Stannard и соавторов возникает в 100% случаев после консервативного лечения и в 18%-100% после оперативного. При этом нестабильность хотя бы в одной из плоскостей в среднем возникает у 42% пациентов [63].
Результаты лечения пациентов с вывихами в коленном суставе
Результаты лечения пациентов с вывихами в коленном суставе достаточно трудно подвергать систематическому анализу ввиду значительной гетерегонности возможных повреждений [41]. Действительно, вывихи могут варьировать от неконтактного трех-связочного повреждения, которое спонтанно исходит в выздоровление, до высокоэнергетических повреждений при дорожно-транспортных происшествиях с серьезным поражением сосудов и нервов. Тем не менее, систематические анализы по этой теме существуют, но мы еще раз подчеркнем, что при интерпретации этих данным не стоит забывать о гетерогенности повреждений.
Levy и соавторы выполнили систематический обзор 413 статей по этой теме. Они оценивали исследования, сравнивающие сравнивающих хирургическое лечение и консервативное лечение [4, 53, 54], восстановление и реконструкцию [45, 64], раннее и отсроченное хирургическое лечение [19, 27, 44, 70, 71].
Из 4 исследований, сравнивающих оперативное и консервативное лечение [4, 53, 54, 75], одно являлось мета-анализом работ, опубликованных до 2000 г [4]. В трех оставшихся работах для оценки исходов лечения использовались шкалы Lysholm и IKDC. Оказалось, что хирургическое лечение давало лучшие результаты по шкале Lysholm, но статистически значимое преимущество было зарегистрировано только в одном из исследований. По шкале IKDC результаты также были лучше в группах оперативного лечения [53, 75]. Хирургическая стабилизация также позволила улучшить показатели восстановления трудоспособности и возврата к спорту при объединении результатов исследований.
В двух исследованиях, сравнивающих восстановление с реконструкцией [64, 45] непосредственное сшивание крестообразных связок привело к значительному снижению амплитуды движений, большей частоте положительных симптомов заднего выдвижного ящика (симптомы заднего «провисания» или sag-симптомы), и менее полному восстановлению функции в сравнении с уровнем, предшествовавшим травме [45]. Частота неудач после восстановления заднелатерального угла также была выше, чем после реконструкции [64].
В целом можно отметить, что большинство авторов под ранними хирургическими вмешательствами подразумевали те, которые выполнялись в срок до 3 недель после травмы. Оказалось, что раннее хирургическое лечение позволяет улучшить ряд параметров [19, 44, 45, 70, 71]. Однако ориентироваться на эти результаты следует с большой осторожностью, так как показания и противопоказания к раннему или отсроченному хирургическому лечению в первую очередь определяются состоянием мягких тканей.
Engebretsen и соавторы [8] выполнили прекрасное проспективное когортное исследование с наблюдением в течение двух лет после реконструктивного лечения пациентов с вывихами в коленном суставе. Критериями включения являлись: травма обеих передней и задней крестообразных связок, а также повреждения медиального и/или латерального комплекса. Пациенты получали лечение в виде хирургической реконструкции в течение 2 недель с даты травмы при отсутствии противопоказаний, обусловленных другими повреждениями. Авторы использовали как аутотрасплантанты, так и аллотрансплантаты. При этом на протяжении исследования имелась тенденция к постепенному увеличению частоты использования аутотрансплантата, который в конце работы стал превалирующим материалом. Примерно у половины пациентов вывих в коленном уставе носил высокоэнергетический характер. Из 121 пациента только 85 пациентов были отслежены с достаточным периодом наблюдения. Медианное значение по шкале Lysholm составило 83 балла, а медианное значение по шкале Tegner– 5 баллов. Авторы обнаружили, что травмы высокоэнергетического характера и травмы с повреждением четырех связок дают худшие результаты по сравнению с низкоэнергетическими травмами и травмами с повреждением трех связок.
Однако в настоящее время нет рандомизированных контроллируемых исследований, изучающих различные протоколы лечения пациентов с вывихами в коленном суставе. Во многом отсутствие исследований обусловлено тяжестью самой травмы, которая по ряду причин делает корректную рандомизацию невозможной [41]. В целом стоит признать, что научное обоснование лечения пациентов достаточно слабое, а целесообразным стоит признать проведение исследований по определению оптимальной тактики лечения и выявлению прогностических факторов. Решение этих задач возможно только путем проведения крупных мультицентровых исследований.
Резюме
Прогресс хирургических методик, в том числе и появление способов анатомической реконструкции, привел к значительному улучшению результатов лечения пациентов с множественными повреждениями коленного сустава. В настоящее время рекомендации включают в себя:
- Определение лодыжечно-плечевого индекса у каждого пациента.
- Раннее хирургическое лечение (не позднее трех недель с момента травмы).
- Применение алло- и аутоматериалов для реконструкции.
- Реконструкцию, а не только лишь восстановление малоберцовой коллатеральной связки и заднелатерального угла. При этом целесообразна комбинация реконструкции и восстановления там, где это возможно.
- Реконструкцию передней и задней крестообразных связок и восстановление и/или реконструкцию медиальной коллатеральной связки и заднемедиального угла в зависимости от варианта их повреждения и качества связок.

